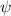 von nichtwechselwirkenden Teilchen, beispielsweise für ein
Mehrelektronenatom, gilt das folgende Postulat:
von nichtwechselwirkenden Teilchen, beispielsweise für ein
Mehrelektronenatom, gilt das folgende Postulat:
Bisher haben wir uns vorwiegend mit der quantenmechanischen Beschreibung des einfachsten Atoms, des Wasserstoffatoms, beschäftigt und teilweise diese Betrachtungen auf andere Systeme, in denen ein einzelnes Elektron um einen positiven Kern kreist, erweitert. In diesem Kapitel widmen wir uns nun Atomen mit mehreren Elektronen. Eine exakte Lösung der Schrödinger-Gleichung ist zwar für das Heliumatom (zwei Elektronen) unter gewissen Annahmen möglich, jedoch für Atome mit mehr als zwei Elektronen aussichtslos. Es existieren aber diverse Näherungslösungen bzw. daraus abgeleitete angenäherte Modelle für Mehrelektronenatome. Wir beschäftigen uns hier mit einem der einfachsten Modelle, dem Schalenmodell, welches sich direkt aus der Verallgemeinerung der Resultate des Wasserstoffatoms ergibt.
Als erstes befassen wir uns mit der Wellenfunktion von Mehrelektronenatomen. In diesem Zusammenhang formulieren wir das vierte Postulat der Quantenmechanik und gehen auf die sogenannte Austauschsymmetrie ein. Anschliessend folgt das Pauli-Prinzip und die Klassifizierung von Teilchen (Elementarteilchen, Atome, Moleküle, ...) in Fermionen und Bosonen. Ausgehend von diesen Gesetzen befassen wir uns dann mit dem Aufbau von Mehrelektronenatomen. Wir betrachten die Besetzung der elektronischen Zustände, die Berechnung von Gesamtbahndrehimpuls, Gesamtspin und Gesamtdrehimpuls, sowie die Bestimmung des Grundzustands aufgrund der sogenannten Hundschen Regeln.
Für die Wellenfunktion 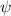 von nichtwechselwirkenden Teilchen, beispielsweise für ein
Mehrelektronenatom, gilt das folgende Postulat:
von nichtwechselwirkenden Teilchen, beispielsweise für ein
Mehrelektronenatom, gilt das folgende Postulat:
Postulat 4 Die Wellenfunktion 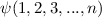 eines Systems aus
eines Systems aus 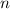 nicht-unterscheidbaren, nicht-wechselwirkenden Teilchen wird durch ein (Tensor-)
Produkt der Wellenfunktionen
nicht-unterscheidbaren, nicht-wechselwirkenden Teilchen wird durch ein (Tensor-)
Produkt der Wellenfunktionen 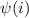 der einzelnen Teilchen beschrieben
der einzelnen Teilchen beschrieben
Die sogenannte Austauschsymmetrie präzisiert die Eigenschaften der Mehrteilchenwellenfunktion (16.1) bzgl. der Vertauschung von Teilchen bzw. ihrer Indizes.
Wir betrachten zwei Elektronen (ohne Spin) am Ort 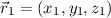 und
und
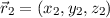 , die sich im Coulomb-Feld eines Atomkerns der Ladung
, die sich im Coulomb-Feld eines Atomkerns der Ladung 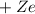 bewegen (siehe Abb. 16.1).
bewegen (siehe Abb. 16.1).
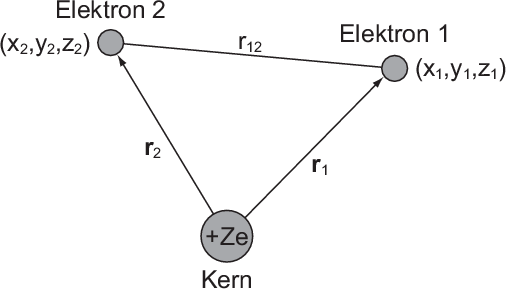
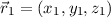 und
und 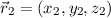 im Coulomb-Feld eines sich im Ursprung des Koordinatensystems befindenden
Atomkerns der Ladung
im Coulomb-Feld eines sich im Ursprung des Koordinatensystems befindenden
Atomkerns der Ladung 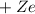 .
.Der Kern wird als fest betrachtet und befindet sich im Ursprung des
Koordinatensystems. Die potentielle Energie der Elektronen setzt sich zusammen aus
der potentiellen Energie 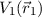 und
und 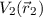 im Coulomb-Feld des Atomkerns
im Coulomb-Feld des Atomkerns
und der potentiellen Energie 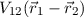 der Coulomb-Wechselwirkung zwischen
den beiden Elektronen
der Coulomb-Wechselwirkung zwischen
den beiden Elektronen
Die kinetische Energie 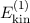 und
und 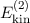 der beiden Elektronen ist gegeben
durch
der beiden Elektronen ist gegeben
durch
Demzufolge lautet die Hamilton-Funktion 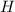 für das Zweielektronensystem
für das Zweielektronensystem
Der entsprechende Hamilton-Operator 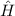 ist gegeben durch
ist gegeben durch
Dieser Hamilton-Operator 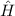 wirkt auf die Wellenfunktion
wirkt auf die Wellenfunktion 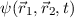 , welche den
Zustand des Zweiteilchensystems beschreibt, wobei
, welche den
Zustand des Zweiteilchensystems beschreibt, wobei 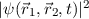 die Wahrscheinlichkeit
ist, das Elektron 1 zur Zeit
die Wahrscheinlichkeit
ist, das Elektron 1 zur Zeit 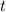 im Volumenelement
im Volumenelement 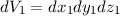 am Ort
am Ort 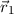 und gleichzeitig das Elektron 2 im Volumenelement
und gleichzeitig das Elektron 2 im Volumenelement 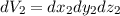 am Ort
am Ort
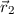 anzutreffen. Da die potentielle Energie
anzutreffen. Da die potentielle Energie 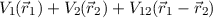 die Zeit
die Zeit 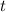 nicht explizit enthält, existieren stationäre Zustände, d.h. es
gilt
nicht explizit enthält, existieren stationäre Zustände, d.h. es
gilt
wobei 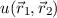 Lösung der zeitunabhängigen Schrödinger-Gleichung
Lösung der zeitunabhängigen Schrödinger-Gleichung
ist. Das Lösen dieser Gleichung ist erheblich erschwert durch den Wechselwirkungsterm
 . Aus diesem Grund ist auch das Postulat 4 nicht anwendbar, da die
beiden Elektronen nicht unabhängig voneinander sind. Wir werden hier diese
Wechselwirkung vernachlässigen. In dieser Näherung ist dann der Hamilton-Operator
als Summe zweier unabhängiger Hamilton-Operatoren darstellbar. Jedes Elektron
hat dann seine eigene Schrödinger-Gleichung mit den Lösungen
. Aus diesem Grund ist auch das Postulat 4 nicht anwendbar, da die
beiden Elektronen nicht unabhängig voneinander sind. Wir werden hier diese
Wechselwirkung vernachlässigen. In dieser Näherung ist dann der Hamilton-Operator
als Summe zweier unabhängiger Hamilton-Operatoren darstellbar. Jedes Elektron
hat dann seine eigene Schrödinger-Gleichung mit den Lösungen 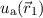 bzw.
bzw. 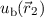
Die Gesamtwellenfunktion 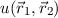 lässt sich dann in Übereinstimmung mit
Postulat 4 als Produkt der beiden Funktionen
lässt sich dann in Übereinstimmung mit
Postulat 4 als Produkt der beiden Funktionen 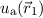 und
und 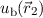 schreiben und
gehört zum Energiewert
schreiben und
gehört zum Energiewert 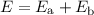 .
. 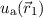 und
und 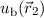 sind dabei gegeben
durch die Eigenfunktionen
sind dabei gegeben
durch die Eigenfunktionen  des Wasserstoffatoms.
des Wasserstoffatoms.
Jedoch folgt aus der Unschärferelation, dass man die Bewegung eines Elektrons nicht
genau verfolgen kann. Als Konsequenz ergibt sich daraus, dass man die beiden
Elektronen im betrachteten Atom nicht auseinanderhalten bzw. unterscheiden kann.
Das hat zur Folge, dass sich bei der Vertauschung der beiden Elektronen,
repräsentiert durch die Vertauschung der beiden Indizes 1 und 2, die
Wahrscheinlichkeitsdichte 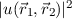 nicht ändern darf. Dies ist die Forderung der
Austauschsymmetrie.
nicht ändern darf. Dies ist die Forderung der
Austauschsymmetrie.
Die Produktwellenfunktion 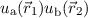 erfüllt diese Forderung nicht, denn
erfüllt diese Forderung nicht, denn
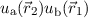 ist nicht die selbe Funktion wie
ist nicht die selbe Funktion wie 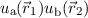 , es sei denn die
Quantenzahlen
, es sei denn die
Quantenzahlen 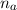 ,
, 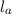 ,
, 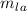 stimmen paarweise mit den Quantenzahlen
stimmen paarweise mit den Quantenzahlen
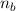 ,
, 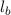 ,
, 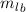 überein. Andererseits ist in der Näherung
überein. Andererseits ist in der Näherung 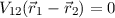 die Produktwellenfunktion
die Produktwellenfunktion 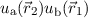 mit vertauschten Indizes 1 und 2
auch eine Eigenfunktion des Hamilton-Operators
mit vertauschten Indizes 1 und 2
auch eine Eigenfunktion des Hamilton-Operators 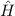 zum selben Eigenwert
zum selben Eigenwert
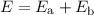 . Diese Tatsache können wir zur Konstruktion von Eigenfunktion
ausnützen, welche die Austauschsymmetrie erfüllen und den Zustand des
Zweielektronensystems beschreiben, indem wir Linearkombinationen von
. Diese Tatsache können wir zur Konstruktion von Eigenfunktion
ausnützen, welche die Austauschsymmetrie erfüllen und den Zustand des
Zweielektronensystems beschreiben, indem wir Linearkombinationen von
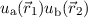 und
und 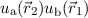 bilden. Diese sind nach Satz 9.4 wiederum
Eigenfunktionen von
bilden. Diese sind nach Satz 9.4 wiederum
Eigenfunktionen von 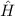 zum selben Eigenwert
zum selben Eigenwert 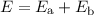 . Es ergeben sich dann
die beiden folgenden normierten Linearkombinationen der Produktwellenfunktionen
. Es ergeben sich dann
die beiden folgenden normierten Linearkombinationen der Produktwellenfunktionen
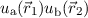 und
und 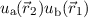 , welche der Forderung der Austauschsymmetrie
genügen
, welche der Forderung der Austauschsymmetrie
genügen
wobei die symmetrische Linearkombination 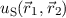 bei der Vertauschung
der beiden Indizes 1 und 2 unverändert bleibt und die antisymmetrische
Linearkombination
bei der Vertauschung
der beiden Indizes 1 und 2 unverändert bleibt und die antisymmetrische
Linearkombination 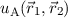 nur das Vorzeichen wechselt. Demzufolge
bleiben
nur das Vorzeichen wechselt. Demzufolge
bleiben 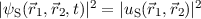 und
und 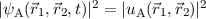 bei
der Vertauschung der Indizes 1 und 2 unverändert und die Forderung der
Austauschsymmetrie ist gewährleistet.
bei
der Vertauschung der Indizes 1 und 2 unverändert und die Forderung der
Austauschsymmetrie ist gewährleistet.
Wir weisen an dieser Stelle darauf hin, dass in der Realität aufgrund des Pauli-Prinzips (siehe Abschnitt 16.2) für Elektronen nicht beide Möglichkeiten (16.13) und (16.14), d.h. symmetrische und antisymmetrische Wellenfunktion, zugelassen sind, sondern Elektronen eine antisymmetrische Wellenfunktion haben müssen.
Die Forderung der Austauschsymmetrie muss auch im Fall von zwei wechselwirkender
Elektronen erfüllt sein, denn diese lassen sich genau so wenig unterscheiden wie
unabhängige Elektronen. Allerdings kann man dann nicht mehr mit den im
vorangegangen Abschnitt benützten Produktwellenfunktionen operieren. Ebenfalls sind
auch noch die Spinkoordinaten 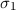 und
und 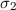 in die Wellenfunktion einzubeziehen.
Die Gesamtwellenfunktion inkl. Spin muss dann entweder symmetrisch oder
antisymmetrisch sein, wenn die Forderung der Austauschsymmetrie erfüllt sein soll
bzw. ist, wie erwähnt, für Elektronen (mit Spin) nach dem Pauli-Prinzip
(siehe Abschnitt 16.2) nur eine antisymmetrische Gesamtwellenfunktion
zugelassen.
in die Wellenfunktion einzubeziehen.
Die Gesamtwellenfunktion inkl. Spin muss dann entweder symmetrisch oder
antisymmetrisch sein, wenn die Forderung der Austauschsymmetrie erfüllt sein soll
bzw. ist, wie erwähnt, für Elektronen (mit Spin) nach dem Pauli-Prinzip
(siehe Abschnitt 16.2) nur eine antisymmetrische Gesamtwellenfunktion
zugelassen.
Zum Abschluss dieses Abschnitts formulieren wir die Forderung der Austauschsymmetrie allgemein:
Die Wellenfunktion 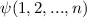 eines Systems aus
eines Systems aus 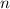 (wechselwirkenden) Teilchen
(Elektronen) erfüllt die Austauschsymmetrie, wenn beim beliebigen Tausch zweier
Teilchen (Elektronen) die Wahrscheinlichkeitsdichte
(wechselwirkenden) Teilchen
(Elektronen) erfüllt die Austauschsymmetrie, wenn beim beliebigen Tausch zweier
Teilchen (Elektronen) die Wahrscheinlichkeitsdichte 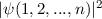 unverändert
bleibt.
unverändert
bleibt.
Es sei bemerkt, dass diese Forderung der Austauschsymmetrie auch in diesem allgemeinen Fall durch die Konstruktion von symmetrischen (bleiben unverändert bei der Vertauschung zweier Teilchen) und antisymmetrischen (ändern das Vorzeichen bei der Vertauschung zweier Teilchen) Wellenfunktionen erfüllt werden kann. Wir weisen zudem darauf hin, dass die Existenz von symmetrischen und antisymmetrischen Wellenfunktionen sich in der Klassifizierung der Teilchen in Fermionen und Bosonen widerspiegelt (siehe Abschnitt 16.3).
Wolfgang Pauli formulierte 1925 das berühmte Pauli-Prinzip, auch Paulisches Ausschlussprinzip genannt. Es lautet folgendermassen:
Ein System von Elektronen wird durch eine antisymmetrische Wellenfunktion beschrieben.
Diese allgemeine und abstrakte Formulierung wird anschaulicher, wenn man sie auf
das in Abschnitt 16.1.2 betrachtete Beispiel von zwei Elektronen anwendet, deren
Wechselwirkung vernachlässigt wird. Nach dem Pauli-Prinzip wird dieses System
durch die antisymmetrische Wellenfunktion 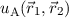 beschrieben, welche
nach (16.14) gegeben ist durch
beschrieben, welche
nach (16.14) gegeben ist durch
Diese Funktion verschwindet, wenn 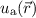 und
und 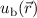 die selbe Funktion darstellen,
d.h. wenn die vier Quantenzahlen
die selbe Funktion darstellen,
d.h. wenn die vier Quantenzahlen 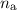 ,
, 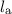 ,
, 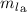 und
und 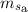 des einen Elektrons
mit den entsprechenden vier Quantenzahlen
des einen Elektrons
mit den entsprechenden vier Quantenzahlen 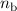 ,
,  ,
,  und
und 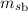 des
anderen Elektrons übereinstimmen. Dies bedeutet, dass ein solcher Zustand des
Zweielektronensystems nicht vorkommt.
des
anderen Elektrons übereinstimmen. Dies bedeutet, dass ein solcher Zustand des
Zweielektronensystems nicht vorkommt.
Diese Beobachtung lässt sich auf ein System bestehend aus beliebig vielen Elektronen verallgemeinern. Daraus ergibt sich folgende alternative Formulierung des Pauli-Prinzips:
Die Elektronenzustände eines Atoms können mit Elektronen nur so besetzt werden, dass nie zwei oder mehr Elektronen in allen Quantenzahlen übereinstimmen.
Das Pauli-Prinzip in dieser Formulierung werden wir uns bei der Betrachtung des Atomaufbaus von Mehrelektronenatomen (siehe Abschnitt 16.4) zunutze machen.
Aufgrund von experimentellen Ergebnissen lassen sich im Allgemeinen Teilchen in zwei Sorten unterteilen, Fermionen und Bosonen, die folgendermassen definiert sind:
Definition 16.1 Wir unterscheiden die beiden folgenden Teilchentypen:
 = 1/2, 3/2, 5/2, ...) wie zum Beispiel
Elektronen, Protonen und Neutronen werden Fermionen genannt
und werden durch eine antisymmetrische Wellenfunktion beschrieben.
Fermionen erfüllen das Pauli-Prinzip.
= 1/2, 3/2, 5/2, ...) wie zum Beispiel
Elektronen, Protonen und Neutronen werden Fermionen genannt
und werden durch eine antisymmetrische Wellenfunktion beschrieben.
Fermionen erfüllen das Pauli-Prinzip.
 = 0, 1, 2, ...) wie zum Beispiel
Photonen,
= 0, 1, 2, ...) wie zum Beispiel
Photonen, 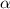 -Teilchen und Helium-Atome werden Bosonen genannt und
werden durch eine symmetrische Wellenfunktion beschrieben. Bosonen
unterliegen nicht dem Pauli-Prinzip.
-Teilchen und Helium-Atome werden Bosonen genannt und
werden durch eine symmetrische Wellenfunktion beschrieben. Bosonen
unterliegen nicht dem Pauli-Prinzip.Neben den Elementarteilchen1
(Elektronen, Protonen und Neutronen) mit Spin 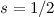 existieren viele Atomkerne
mit halbzahligem Spin zwischen
existieren viele Atomkerne
mit halbzahligem Spin zwischen 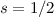 und
und 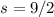 . Die Quantenzahl
. Die Quantenzahl 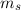 kann
dann jeweils alle halbzahligen Werte zwischen
kann
dann jeweils alle halbzahligen Werte zwischen  und
und 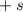 annehmen. Ebenfalls
gibt es auch einige Atomkerne mit ganzzahligem Spin zwischen
annehmen. Ebenfalls
gibt es auch einige Atomkerne mit ganzzahligem Spin zwischen 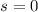 und
und 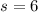 .
Entsprechend kann in diesem Fall die Quantenzahl
.
Entsprechend kann in diesem Fall die Quantenzahl 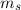 alle ganzzahligen Werte
zwischen
alle ganzzahligen Werte
zwischen  und
und 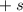 annehmen.
annehmen.
Wir kommen nun zu einer qualitativen Betrachtung des Aufbaus von Mehrelektronenatomen anhand des Schalenmodells. Wie in der Einleitung erwähnt, ergibt sich dieses einfachste Modell direkt aus den Resultaten der Berechnungen zum Wasserstoffatom.
Die Zustände der Elektronen werden ausgehend vom Wasserstoffatommodell
durch die vier Quantenzahlen 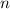 ,
, 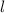 ,
, 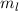 und
und 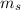 beschrieben, für die
gilt
beschrieben, für die
gilt
Alle Zustände, die zu einer festen Hauptquantenzahl 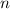 gehören, bilden dabei eine
Schale, alle Zustände, die zu einer festen Bahndrehimpulsquantenzahl
gehören, bilden dabei eine
Schale, alle Zustände, die zu einer festen Bahndrehimpulsquantenzahl 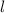 gehören, bilden eine Unterschale. In einer Unterschale hat es demzufolge
Platz für
gehören, bilden eine Unterschale. In einer Unterschale hat es demzufolge
Platz für 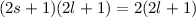 Elektronen und in einer Schale für
Elektronen und in einer Schale für
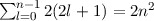 Elektronen.
Elektronen.
Wir kommen nun zur Besetzung der Elektronenzustände und damit der Schalen und Unterschalen von Atomen durch Elektronen. Diese erfolgt nach zwei Prinzipien:
Für die Angabe der Besetzung der Elektronenzustände und damit zur Charakterisierung
des Elektronenzustands eines Atoms verwendet man die folgende Notation: Man gibt
die Hauptquantenzahl 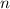 gefolgt von der Bahndrehimpulsquantenzahl
gefolgt von der Bahndrehimpulsquantenzahl 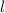 , bezeichnet
durch den zugehörigen Buchstaben, in Klammern an und hochgestellt die Anzahl
Elektronen, welche sich in dieser Unterschale befinden. Zum Beispiel gilt für das
Natriumatom die Elektronenkonfiguration
, bezeichnet
durch den zugehörigen Buchstaben, in Klammern an und hochgestellt die Anzahl
Elektronen, welche sich in dieser Unterschale befinden. Zum Beispiel gilt für das
Natriumatom die Elektronenkonfiguration 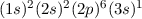 , d.h. es befinden
sich jeweils zwei Elektronen in der
, d.h. es befinden
sich jeweils zwei Elektronen in der  - und
- und 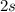 -Unterschale, sechs Elektronen in der
-Unterschale, sechs Elektronen in der
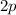 -Unterschale und ein Elektron in der
-Unterschale und ein Elektron in der  -Unterschale.
-Unterschale.
Wir betrachten nun ausgehend vom Wasserstoffatom die Atome des Periodensystems (siehe Abb. 7.3), indem wir die Elektronenzustände schrittweise nach den oben genannten Regeln mit Elektronen besetzen.
Bis zu Argon mit der Ordnungszahl 18 (Ende
Periode2
III) werden die Zustände der Reihe nach besetzt, d.h. das Füllen der Unterschalen
erfolgt in der Reihenfolge 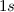 ,
, 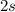 ,
, 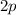 ,
, 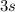 und
und 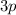 (siehe Tab. 16.1).
(siehe Tab. 16.1).
Ordnungszahl (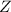 ) ) | Symbol | Bezeichnung | Elektronenkonfiguration |
| 1 | H | Wasserstoff | 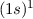 |
| 2 | He | Helium | 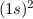 |
| 3 | Li | Lithium | 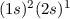 |
| 4 | Be | Beryllium | 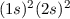 |
| 5 | B | Bor | 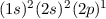 |
| 6 | C | Kohlenstoff | 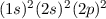 |
| 7 | N | Stickstoff | 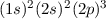 |
| 8 | O | Sauerstoff | 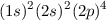 |
| 9 | F | Fluor | 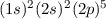 |
| 10 | Ne | Neon | 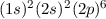 |
| 11 | Na | Natrium | 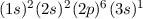 |
| 12 | Mg | Magnesium | 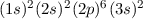 |
| 13 | Al | Aluminium | 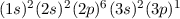 |
| 14 | Si | Silicium | 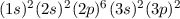 |
| 15 | P | Phosphor | 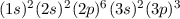 |
| 16 | S | Schwefel | 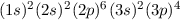 |
| 17 | Cl | Chlor | 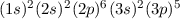 |
| 18 | Ar | Argon | 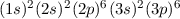 |
Anschliessend erfolgt eine erste Ausnahme. Da die 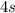 -Unterschale energetisch tiefer
liegt als die
-Unterschale energetisch tiefer
liegt als die 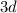 -Unterschale, werden die nächsten beiden Elektronen in der
-Unterschale, werden die nächsten beiden Elektronen in der
 -Unterschale untergebracht (Kalium und Calcium). Es folgt dann mit kleinen
Ausnahmen die Besetzung der
-Unterschale untergebracht (Kalium und Calcium). Es folgt dann mit kleinen
Ausnahmen die Besetzung der 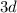 -Unterschale mit zehn weiteren Elektronen
(Scandium bis Zink). Damit sind alle Zustände mit
-Unterschale mit zehn weiteren Elektronen
(Scandium bis Zink). Damit sind alle Zustände mit 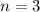 besetzt und die nächsten
sechs Elektronen finden in der
besetzt und die nächsten
sechs Elektronen finden in der 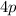 -Unterschale Platz (Gallium bis Krypton). Somit
ist die IV. Periode abgeschlossen.
-Unterschale Platz (Gallium bis Krypton). Somit
ist die IV. Periode abgeschlossen.
Die V. Periode wird analog zur IV. Periode mit Elektronen gefüllt: Zwei
Elektronen finden in der 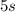 -Unterschale (Rubidium und Strontium) Platz,
mit kleinen Ausnahmen zehn Elektronen in der
-Unterschale (Rubidium und Strontium) Platz,
mit kleinen Ausnahmen zehn Elektronen in der 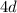 -Unterschale (Yttrium
bis Cadmium) und sechs Elektronen in der
-Unterschale (Yttrium
bis Cadmium) und sechs Elektronen in der 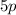 -Unterschale (Indium bis
Xenon).
-Unterschale (Indium bis
Xenon).
Zum Start der VI. Periode werden zwei Elektronen in der 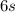 -Unterschale platziert
(Cäsium und Barium). Dann folgen mit kleinen Ausnahmen vierzehn Elektronen in
der
-Unterschale platziert
(Cäsium und Barium). Dann folgen mit kleinen Ausnahmen vierzehn Elektronen in
der 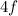 -Unterschale (Lanthan bis Ytterbium) und zehn Elektronen in der
-Unterschale (Lanthan bis Ytterbium) und zehn Elektronen in der
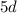 -Unterschale (Lutetium bis Quecksilber) und zum Abschluss der VI. Periode
sechs Elektronen in der
-Unterschale (Lutetium bis Quecksilber) und zum Abschluss der VI. Periode
sechs Elektronen in der 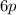 -Unterschale (Thallium bis Radon).
-Unterschale (Thallium bis Radon).
Die Besetzung der Elektronenzustände in der VII. und damit letzten Periode erfolgt
nach dem selben Muster wie bei der VI. Periode. Die 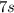 -Unterschale wird
mit zwei Elektronen gefüllt (Francium und Radium), die
-Unterschale wird
mit zwei Elektronen gefüllt (Francium und Radium), die 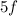 -Unterschale
mit vierzehn (Actinium bis Lawrencium), die
-Unterschale
mit vierzehn (Actinium bis Lawrencium), die 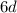 -Unterschale mit zehn
(Rutherfordium bis Copernicium) und die
-Unterschale mit zehn
(Rutherfordium bis Copernicium) und die  -Unterschale mit sechs (Ununtrium bis
Ununoctium).
-Unterschale mit sechs (Ununtrium bis
Ununoctium).
Für einige Gruppen von Atomen existieren in der Literatur spezielle Namen, die wir hier kurz auflisten:
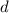 - oder
- oder 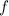 -Unterschalen besetzt werden,
werden Übergangselemente genannt.
-Unterschalen besetzt werden,
werden Übergangselemente genannt.
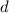 -Unterschalen
besetzt werden, heissen Übergangsmetalle. Die Atome der
-Unterschalen
besetzt werden, heissen Übergangsmetalle. Die Atome der 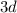 -Unterschale
(Scandium bis Zink) erhalten den Namen Eisengruppe, die Atome der
-Unterschale
(Scandium bis Zink) erhalten den Namen Eisengruppe, die Atome der
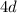 -Unterschale (Yttrium bis Cadmium) Palladiumgruppe und die Atome
der
-Unterschale (Yttrium bis Cadmium) Palladiumgruppe und die Atome
der 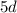 -Unterschale (Lutetium bis Quecksilber) Platingruppe.
-Unterschale (Lutetium bis Quecksilber) Platingruppe.
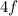 -Unterschale nennt man
Lanthanoide oder seltene Erden und die Atome Actinium bis Lawrencium
der
-Unterschale nennt man
Lanthanoide oder seltene Erden und die Atome Actinium bis Lawrencium
der 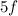 -Unterschale Actinoide.
-Unterschale Actinoide.Allgemein bestimmen die äussersten Elektronen die chemischen Eigenschaften eines Atoms. Aus diesem Grund haben Atome, welche in der selben Gruppe des Periodensystems positioniert sind, ähnliche chemische Eigenschaften. Auf die Eigenschaften der Atome der ersten und letzten Gruppe gehen wir hier beispielhaft ein.
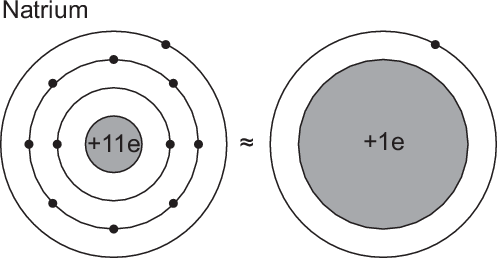
Die Alkali-Atome Lithium bis Francium befinden sich in der ersten Gruppe des Periodensystems und besitzen ein Elektron in der äussersten Schale. Auf das äusserste Elektron wirkt aufgrund der Abschirmung der anderen Elektronen eine reduzierte und relativ geringe Kernladung. Deshalb kann das äusserste Elektron relativ leicht vom Atom getrennt werden. Aus diesem Grund können Alkali-Atome angenähert durch das Wasserstoffatommodell beschrieben werden (siehe Abb. 16.2). Dies zeigt sich auch in Experimenten, die Eigenschaften von Alkali-Atomen sind denen von Wasserstoff sehr ähnlich. Z.B. sind die Atome in dieser Gruppe chemisch sehr reaktiv. Dennoch unterscheiden sich die Alkali-Atome vom Wasserstoffatom in einem wesentlichen Punkt, Wasserstoff ist weder fest noch zeigt er Eigenschaften von Metallen. Dies ist auch der Grund, weshalb Wasserstoff, obwohl es im Periodensystem auch in der ersten Gruppe aufgeführt wird, nicht zu den Alkali-Atomen gezählt wird.
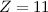 ).
).Zu den Edelgasen gehören die sieben Atome der achten und letzten Gruppe des
Periodensystems, d.h. Helium, Neon, Argon, Krypton, Xenon, Radon und
Ununoctium. Sie zeichnen sich alle durch abgeschlossene Unterschalen aus, d.h. alle
möglichen Zustände in der jeweiligen Unterschale sind mit Elektronen voll besetzt.
Zum Beispiel haben in der  -Unterschale zwei, in der
-Unterschale zwei, in der 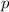 -Unterschale sechs, in
der
-Unterschale sechs, in
der 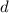 -Unterschale zehn und in der
-Unterschale zehn und in der 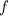 -Unterschale vierzehn Elektronen
Platz. Die Elektronen in einer solchen abgeschlossenen Unterschale sind
stark an den Atomkern gebunden, da die Kernladung nur schwach von den
Elektronen in niedrigeren Schalen abgeschirmt wird. Aus diesem Grund sind
Edelgase im Vergleich zu anderen Atomen chemisch inaktiv. Eine weitere
Eigenschaft von abgeschlossenen Unterschalen ist, dass ihr Gesamtbahndrehimpuls
-Unterschale vierzehn Elektronen
Platz. Die Elektronen in einer solchen abgeschlossenen Unterschale sind
stark an den Atomkern gebunden, da die Kernladung nur schwach von den
Elektronen in niedrigeren Schalen abgeschirmt wird. Aus diesem Grund sind
Edelgase im Vergleich zu anderen Atomen chemisch inaktiv. Eine weitere
Eigenschaft von abgeschlossenen Unterschalen ist, dass ihr Gesamtbahndrehimpuls
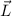 , ihr Gesamtspin
, ihr Gesamtspin 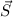 und ihr Gesamtdrehimpuls
und ihr Gesamtdrehimpuls 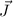 verschwinden (siehe
Abschnitt 16.4.2).
verschwinden (siehe
Abschnitt 16.4.2).
Bei der Bestimmung des Gesamtbahndrehimpulses, des Gesamtspins und des
Gesamtdrehimpulses für ein Mehrelektronenatom unterscheiden wir die beiden
Fälle Russell-Saunders-Kopplung und 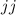 -Kopplung. Im ersten Fall ist die
Coulomb-Wechselwirkung viel grösser als die Spin-Bahn-Kopplung und im
zweiten Fall ist die Coulomb-Wechselwirkung viel kleiner als die Summe aller
Spin-Bahn-Kopplungen der einzelnen Elektronen. Wir gehen nun genauer auf die
beiden Fälle ein:
-Kopplung. Im ersten Fall ist die
Coulomb-Wechselwirkung viel grösser als die Spin-Bahn-Kopplung und im
zweiten Fall ist die Coulomb-Wechselwirkung viel kleiner als die Summe aller
Spin-Bahn-Kopplungen der einzelnen Elektronen. Wir gehen nun genauer auf die
beiden Fälle ein:
Bei Mehrelektronenatomen mit nicht zu hoher Kernladungszahl 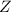 , d.h. bei
leichten Atomen, ist die Coulomb-Wechselwirkung viel grösser als die
Spin-Bahn-Kopplung. In diesem Fall koppeln die Bahndrehimpulse
, d.h. bei
leichten Atomen, ist die Coulomb-Wechselwirkung viel grösser als die
Spin-Bahn-Kopplung. In diesem Fall koppeln die Bahndrehimpulse 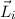 der
einzelnen Elektronen zu einem Gesamtbahndrehimpuls
der
einzelnen Elektronen zu einem Gesamtbahndrehimpuls 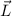 im folgenden
Sinn
im folgenden
Sinn
wobei 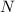 die Anzahl der Elektronen bezeichnet. Analog koppeln die
Spins
die Anzahl der Elektronen bezeichnet. Analog koppeln die
Spins 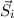 der einzelnen Elektronen zu einem Gesamtspin
der einzelnen Elektronen zu einem Gesamtspin 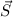 , d.h. es
gilt
, d.h. es
gilt
Wie beim Wasserstoffatom wechselwirken aufgrund der Spin-Bahn-Kopp-lung
der resultierende Gesamtbahndrehimpuls 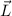 mit dem Gesamtspin
mit dem Gesamtspin 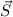 und
bestimmen so den Gesamtdrehimpuls
und
bestimmen so den Gesamtdrehimpuls 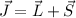 . Der Betrag der Drehimpulse
. Der Betrag der Drehimpulse
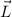 ,
, 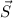 und
und 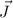 ist dabei auf die gleiche Art und Weise wie beim Wasserstoffatom
quantisiert. Sie sind bestimmt durch die Quantenzahlen
ist dabei auf die gleiche Art und Weise wie beim Wasserstoffatom
quantisiert. Sie sind bestimmt durch die Quantenzahlen 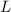 ,
, 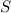 und
und
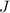 3
auf folgende Art
3
auf folgende Art
wobei die Quantenzahlen 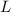 ,
, 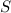 und
und 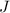 die folgenden Werte annehmen
können
die folgenden Werte annehmen
können
wobei 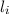 und
und 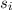 die Bahndrehimpulsquantenzahlen bzw. Spinquantenzahlen
der einzelnen Elektronen bezeichnen und die
die Bahndrehimpulsquantenzahlen bzw. Spinquantenzahlen
der einzelnen Elektronen bezeichnen und die 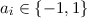 so gewählt sind,
dass
so gewählt sind,
dass 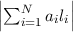 bzw.
bzw.  minimal werden. Zum Beispiel bedeutet
dies im Fall
minimal werden. Zum Beispiel bedeutet
dies im Fall 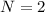
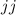 -Kopplung
-Kopplung
Bei Mehrelektronenatomen mit hoher Kernladungszahl 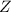 , d.h. bei
schweren Atomen, ist die Coulomb-Wechselwirkung viel kleiner als die
Spin-Bahn-Kopplung der einzelnen Elektronen. Es ist dann nicht mehr
möglich einen Gesamtbahndrehimpuls
, d.h. bei
schweren Atomen, ist die Coulomb-Wechselwirkung viel kleiner als die
Spin-Bahn-Kopplung der einzelnen Elektronen. Es ist dann nicht mehr
möglich einen Gesamtbahndrehimpuls 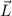 und einen Gesamtspin
und einen Gesamtspin 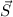 zu definieren, sondern die Bahndrehimpulse
zu definieren, sondern die Bahndrehimpulse 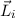 und Spins
und Spins 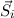 der
einzelnen Elektronen koppeln einzeln zu einem Gesamtdrehimpuls
der
einzelnen Elektronen koppeln einzeln zu einem Gesamtdrehimpuls 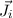 der
einzelnen Elektronen und diese wiederum zu einem Gesamtdrehimpuls
der
einzelnen Elektronen und diese wiederum zu einem Gesamtdrehimpuls 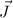 gemäss
gemäss
Es sei an dieser Stelle bemerkt, dass in der Realität bei den meisten Atomen
eine Mischform zwischen Russell-Saunders- und 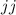 -Kopplung vorliegt. Zur
Veranschaulichung besprechen wir nun die Russell-Saunders-Kopplung für ein Atom
mit zwei Elektronen.
-Kopplung vorliegt. Zur
Veranschaulichung besprechen wir nun die Russell-Saunders-Kopplung für ein Atom
mit zwei Elektronen.
Wir betrachten ein Atom mit zwei Elektronen, welche durch die
Bahndrehimpulsquantenzahlen 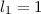 und
und 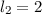 , sowie die Spinquantenzahlen
, sowie die Spinquantenzahlen
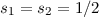 beschrieben werden. Die Gesamtbahndrehimpulsquantenzahl
beschrieben werden. Die Gesamtbahndrehimpulsquantenzahl 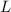 kann in diesem Fall die folgenden drei Werte annehmen
kann in diesem Fall die folgenden drei Werte annehmen
und die Gesamtspinquantenzahl 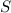 die beiden Werte
die beiden Werte
Damit ergeben sich für die Gesamtdrehimpulsquantenzahl 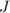 fünf Möglichkeiten
fünf Möglichkeiten
Für die Zustände von Mehrelektronenatomen verwendet man im Vergleich zum Wasserstoffatom eine geringfügig angepasste Notation. In Anlehnung an (14.41) gilt für Mehrelektronenatome:
Ein Zustand eines Mehrelektronenatoms mit Gesamtbahndrehimpulsquantenzahl 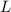 ,
Gesamtspinquantenzahl
,
Gesamtspinquantenzahl 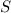 und Gesamtdrehimpulsquantenzahl
und Gesamtdrehimpulsquantenzahl 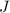 erhält folgende
Bezeichnung
erhält folgende
Bezeichnung
wobei für 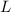 jeweils der entsprechende Grossbuchstabe
jeweils der entsprechende Grossbuchstabe 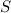 (
(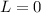 ),
), 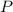 (
(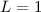 ),
),
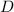 (
(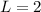 ), ... einzusetzen ist. Bei Atomen mit einem einzigen Elektron in der
äussersten Unterschale wird die Hauptquantenzahl
), ... einzusetzen ist. Bei Atomen mit einem einzigen Elektron in der
äussersten Unterschale wird die Hauptquantenzahl  dieses Elektrons der
Bezeichnung vorangestellt.
dieses Elektrons der
Bezeichnung vorangestellt.
Es sei bemerkt, dass im Fall 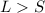 der vor dem Buchstaben hochgestellte Index
der vor dem Buchstaben hochgestellte Index
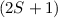 gerade die Multiplizität des Zustands angibt, d.h. die Zahl der
Möglichkeiten den Gesamtbahndrehimpuls
gerade die Multiplizität des Zustands angibt, d.h. die Zahl der
Möglichkeiten den Gesamtbahndrehimpuls 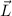 und den Gesamtspin
und den Gesamtspin 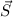 zum
Gesamtdrehimpuls
zum
Gesamtdrehimpuls 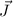 zu kombinieren. Dabei werden die zu den drei Werten
zu kombinieren. Dabei werden die zu den drei Werten 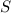 =
0, 1/2, 1 der Gesamtspinquantenzahl zugehörenden Zustände mit Namen
versehen:
=
0, 1/2, 1 der Gesamtspinquantenzahl zugehörenden Zustände mit Namen
versehen:
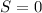 ist die Multiplizität
ist die Multiplizität 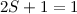 und es existiert folglich nur
ein Zustand mit
und es existiert folglich nur
ein Zustand mit 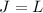 den man Singulett-Zustand nennt.
den man Singulett-Zustand nennt.
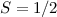 existieren
existieren 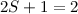 mögliche Zustände mit
mögliche Zustände mit
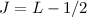 und
und 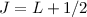 . Diese bilden zusammen ein Dublett.
. Diese bilden zusammen ein Dublett.
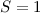 gibt es
gibt es 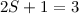 mögliche Zustände mit
mögliche Zustände mit 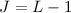 ,
,
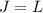 und
und 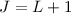 . Diese bilden zusammen ein Triplett.
. Diese bilden zusammen ein Triplett.Im Fall 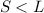 ist die Multiplizität gegeben durch
ist die Multiplizität gegeben durch 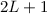 .
.
Zum Abschluss dieses Abschnitts geben wir als Beispiel die Notation für
das Natriumatom an. Nach Tab. 16.1 hat Natrium elf Elektronen mit einer
Elektronenkonfiguration 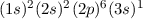 . Die drei Unterschalen
. Die drei Unterschalen 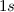 ,
, 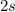 und
und
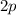 sind abgeschlossen und haben daher verschwindende Quantenzahlen
sind abgeschlossen und haben daher verschwindende Quantenzahlen 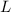 ,
, 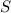 und
und
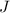 . Daher genügt es das äusserste Elektron, welches sich im Zustand
. Daher genügt es das äusserste Elektron, welches sich im Zustand 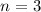 ,
, 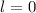 und
und 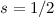 befindet, zu betrachten. Demzufolge gilt für das Natriumatom
befindet, zu betrachten. Demzufolge gilt für das Natriumatom 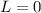 ,
,
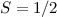 und
und 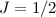 und damit die Bezeichnung
und damit die Bezeichnung 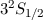 , wobei wir die
Hauptquantenzahl
, wobei wir die
Hauptquantenzahl 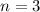 des Zustands des äussersten Elektrons der Bezeichnung
vorangestellt haben.
des Zustands des äussersten Elektrons der Bezeichnung
vorangestellt haben.
Wir haben bisher die Elektronenkonfigurationen der einzelnen Atome kennengelernt,
welche die Atome in ihrem Grundzustand einnehmen (siehe Abschnitt 16.4.1). Jedoch
wissen wir noch nicht welchen Zustand 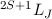 das Atom genau einnimmt.
Insbesondere die Besetzung von nicht abgeschlossenen Schalen ist noch zu
klären.
das Atom genau einnimmt.
Insbesondere die Besetzung von nicht abgeschlossenen Schalen ist noch zu
klären.
Eine Antwort liefern die Hundschen Regeln, die nach dem Physiker Friedrich Hund
benannt sind und auf empirischen Resultaten beruhen. Sie geben an, welche Werte
die Quantenzahlen 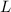 ,
, 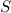 und
und 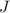 für ein Atom im Grundzustand annehmen. Sie
lauten folgendermassen:
für ein Atom im Grundzustand annehmen. Sie
lauten folgendermassen:
Hundsche Regeln
Im Grundzustand besetzen die Elektronen eines Atoms unter Berücksichtigung des Pauli-Prinzips die Zustände nach den folgenden Regeln:
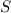 nimmt den maximal möglichen Wert an.
nimmt den maximal möglichen Wert an.
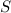 ,
liegt derjenige mit maximaler Gesamtbahndrehimpulsquantenzahl
,
liegt derjenige mit maximaler Gesamtbahndrehimpulsquantenzahl 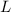 energetisch am tiefsten.
energetisch am tiefsten.
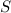 und
maximaler Gesamtbahndrehimpulsquantenzahl
und
maximaler Gesamtbahndrehimpulsquantenzahl 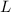 bildet bei weniger als
halbgefüllten Schalen der Zustand mit
bildet bei weniger als
halbgefüllten Schalen der Zustand mit 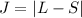 (minimales
(minimales 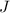 ) den
Grundzustand, sonst der Zustand mit
) den
Grundzustand, sonst der Zustand mit 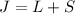 (maximales
(maximales 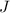 ).
).Es sei bemerkt, dass manchmal auch die in Abschnitt 16.4.1 im Rahmen
der Behandlung der Edelgase angesprochene Regel, dass für abgeschlossene
Unterschalen 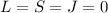 ist, als weitere Hundsche Regel aufgeführt
wird.
ist, als weitere Hundsche Regel aufgeführt
wird.
Wir geben hier eine kurze Motivation der beiden ersten Regeln an und verweisen für genauere Ausführungen auf weiterführende Literatur (z.B. [11]). Dazu benützen wir die am Anfang des Abschnitts 16.4 aufgeführte Regel, dass ein Atom dann einen stabilen Zustand einnimmt, wenn seine Gesamtenergie minimal ist:
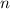 und
und 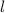 ) zunächst mit ungepaarten Elektronen
derselben
Spinquantenzahl
) zunächst mit ungepaarten Elektronen
derselben
Spinquantenzahl 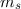 , d.h. mit paralleler Spinausrichtung, besetzt werden
(maximiert Gesamtspinquantenzahl
, d.h. mit paralleler Spinausrichtung, besetzt werden
(maximiert Gesamtspinquantenzahl 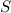 ). Solche Elektronen mit derselben
Spinquantenzahl
). Solche Elektronen mit derselben
Spinquantenzahl 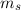 haben aufgrund des Pauli-Prinzips unterschiedliche
Quantenzahlen
haben aufgrund des Pauli-Prinzips unterschiedliche
Quantenzahlen 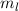 und daher einen maximalen räumlichen Abstand.
Dies hat eine minimale Coulomb-Wechselwirkung (Abstossung) zwischen
den Elektronen zur Folge. Daher liegt der Zustand mit maximaler
Gesamtspinquantenzahl
und daher einen maximalen räumlichen Abstand.
Dies hat eine minimale Coulomb-Wechselwirkung (Abstossung) zwischen
den Elektronen zur Folge. Daher liegt der Zustand mit maximaler
Gesamtspinquantenzahl 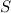 energetisch am tiefsten und wird von den
Elektronen des Atoms im Grundzustand eingenommen.
energetisch am tiefsten und wird von den
Elektronen des Atoms im Grundzustand eingenommen.
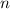 und
und 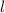 ), dass neben der Bevorzugung paralleler Spins, zuerst der
Zustand mit maximalem
), dass neben der Bevorzugung paralleler Spins, zuerst der
Zustand mit maximalem 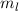 besetzt wird, anschliessend der Zustand
mit
besetzt wird, anschliessend der Zustand
mit 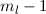 , usw. (maximiert Gesamtbahndrehimpulsquantenzahl
, usw. (maximiert Gesamtbahndrehimpulsquantenzahl 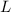 ).
Aufgrund dieser Besetzung sind die Elektronen so weit wir möglich vom
Zentrum und dadurch auch voneinander entfernt. Dies hat wiederum
eine minimale Coulomb-Wechselwirkung (Abstossung) zwischen den
Elektronen zur Folge. Der Effekt ist jedoch geringer als bei den Spins.
Daher liegt unter den Zuständen mit maximaler Gesamtspinquantenzahl
).
Aufgrund dieser Besetzung sind die Elektronen so weit wir möglich vom
Zentrum und dadurch auch voneinander entfernt. Dies hat wiederum
eine minimale Coulomb-Wechselwirkung (Abstossung) zwischen den
Elektronen zur Folge. Der Effekt ist jedoch geringer als bei den Spins.
Daher liegt unter den Zuständen mit maximaler Gesamtspinquantenzahl
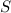 der Zustand mit maximaler Gesamtbahndrehimpulsquantenzahl
der Zustand mit maximaler Gesamtbahndrehimpulsquantenzahl 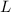 energetisch am tiefsten und wird von den Elektronen des Atoms im
Grundzustand eingenommen.
energetisch am tiefsten und wird von den Elektronen des Atoms im
Grundzustand eingenommen.In Tab. 16.2 sind anhand der genauen Elektronenbesetzung für die Atome Bor bis Neon diese beiden Punkte illustriert4.
| Name | Elektronenkonfiguration | Besetzung der
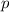 -Unterschale -Unterschale | ||
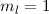 | 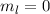 | 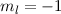 |
||
| Bor | 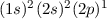 | 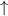 | ||
| Kohlenstoff | 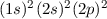 | 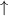 | 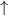 | |
| Stickstoff | 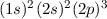 | 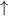 | 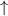 | 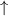 |
| Sauerstoff | 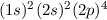 | 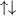 | 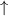 | 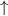 |
| Fluor | 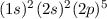 | 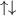 | 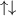 | 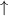 |
| Neon | 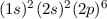 |  |  |  |
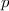 -Unterschale am Beispiel der Atome Bor
bis Neon nach den Hundschen Regeln 1 und 2.
-Unterschale am Beispiel der Atome Bor
bis Neon nach den Hundschen Regeln 1 und 2. 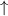 steht dabei für ein
Elektron im „spin-up“-Zustand (
steht dabei für ein
Elektron im „spin-up“-Zustand (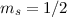 ) und
) und  für ein Elektron im
„spin-down“-Zustand (
für ein Elektron im
„spin-down“-Zustand (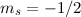 ).
).Wir illustrieren die Hundschen Regeln an den Atomen Wasserstoff bis Neon (siehe Tab. 16.3), wobei wir die Elemente Wasserstoff, Helium, Bor, Kohlenstoff und Stickstoff genauer besprechen:
| Name | 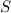 | 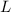 | 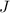 | 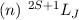 |
| Wasserstoff | 1/2 | 0 | 1/2 | 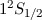 |
| Helium | 0 | 0 | 0 | 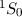 |
| Lithium | 1/2 | 0 | 1/2 | 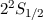 |
| Beryllium | 0 | 0 | 0 | 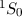 |
| Bor | 1/2 | 1 | 1/2 | 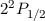 |
| Kohlenstoff | 1 | 1 | 0 | 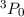 |
| Stickstoff | 3/2 | 0 | 3/2 | 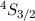 |
| Sauerstoff | 1 | 1 | 2 | 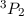 |
| Fluor | 1/2 | 1 | 3/2 | 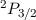 |
| Neon | 0 | 0 | 0 | 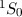 |
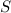 ,
, 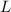 und
und 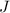 und die spektroskopische
Notation
und die spektroskopische
Notation 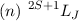 des Grundzustands für die Atome Wasserstoff bis Neon
nach den Hundschen Regeln.
des Grundzustands für die Atome Wasserstoff bis Neon
nach den Hundschen Regeln.Beim Wasserstoffatom ist die Situation am einfachsten. Wir haben ein
Elektron in der 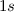 -Unterschale, das entweder den „spin up“- (
-Unterschale, das entweder den „spin up“- (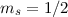 )
oder den „spin-down“- (
)
oder den „spin-down“- (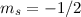 ) Zustand einnehmen kann. Damit
resultieren die Quantenzahlen
) Zustand einnehmen kann. Damit
resultieren die Quantenzahlen 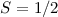 ,
, 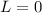 und
und 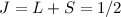 und der Grundzustand
und der Grundzustand 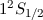 .
.
Die beiden Elektronen besetzen im Grundzustand die beiden möglichen
Zustände in der 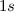 -Unterschale. Für abgeschlossene Unterschalen
verschwinden die drei Quantenzahl
-Unterschale. Für abgeschlossene Unterschalen
verschwinden die drei Quantenzahl 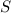 ,
, 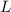 und
und 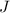 und wird erhalten den
Grundzustand
und wird erhalten den
Grundzustand 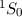 .
.
Für die abgeschlossenen Unterschalen 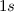 und
und 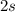 gilt
gilt 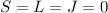 und es genügt das einzelne Elektron in der
und es genügt das einzelne Elektron in der 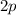 -Unterschale zu betrachten.
Nach den ersten beiden Hundschen Regeln nimmt es den Zustand
-Unterschale zu betrachten.
Nach den ersten beiden Hundschen Regeln nimmt es den Zustand 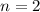 ,
,
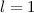 ,
, 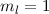 und
und 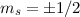 ein. Demzufolge gilt
ein. Demzufolge gilt 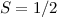 und
und
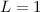 und da die
und da die 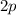 -Unterschale weniger als halb gefüllt ist, ergibt sich
nach der dritten Hundschen Regel
-Unterschale weniger als halb gefüllt ist, ergibt sich
nach der dritten Hundschen Regel 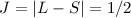 . Somit lautet der
Grundzustand für das Boratom
. Somit lautet der
Grundzustand für das Boratom 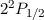 .
.
Wie beim Boratom haben wir nur die beiden Elektronen in der
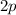 -Unter-schale zu betrachten (
-Unter-schale zu betrachten (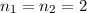 und
und 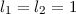 ). Nach
der ersten Hundschen Regel haben sie parallelen Spin (beide
). Nach
der ersten Hundschen Regel haben sie parallelen Spin (beide 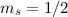 oder beide
oder beide 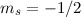 ) und damit gilt
) und damit gilt 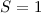 . Die zweite Hundsche
Regel legt nun die letzte Quantenzahl
. Die zweite Hundsche
Regel legt nun die letzte Quantenzahl 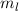 fest. Unter Berücksichtigung
des Pauli-Prinzips nimmt
fest. Unter Berücksichtigung
des Pauli-Prinzips nimmt 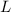 für
für 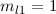 und
und 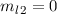 den maximalen
Wert 1 an. Für die letzte Quantenzahl erhalten wir nach der dritten
Hundschen Regel
den maximalen
Wert 1 an. Für die letzte Quantenzahl erhalten wir nach der dritten
Hundschen Regel  und somit für das Kohlenstoffatom
den Grundzustand
und somit für das Kohlenstoffatom
den Grundzustand 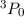 .
.
Wiederum können wir uns auf die drei Elektronen in der 2p-Unterschale
konzentrieren (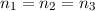 und
und 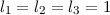 ). Die erste Hundsche
Regel verlangt wiederum parallele Spins, womit
). Die erste Hundsche
Regel verlangt wiederum parallele Spins, womit 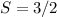 ist. Nach
dem Pauli-Prinzip müssen sie die Zustände zu
ist. Nach
dem Pauli-Prinzip müssen sie die Zustände zu 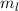 = -1, 0 und 1
besetzen. Wodurch nur die Möglichkeit
= -1, 0 und 1
besetzen. Wodurch nur die Möglichkeit 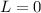 bleibt. Die Unterschale
ist halb gefüllt und daher folgt nach der dritten Hundschen Regel
bleibt. Die Unterschale
ist halb gefüllt und daher folgt nach der dritten Hundschen Regel
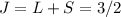 . Stickstoff besitzt also den Grundzustand
. Stickstoff besitzt also den Grundzustand 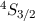 .
.
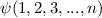 eines
Systems aus
eines
Systems aus 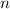 nicht-unterscheidbaren, nicht-wechselwirkenden Teilchen wird
durch ein (Tensor-) Produkt der Wellenfunktionen
nicht-unterscheidbaren, nicht-wechselwirkenden Teilchen wird
durch ein (Tensor-) Produkt der Wellenfunktionen 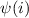 der einzelnen Teilchen
beschrieben
der einzelnen Teilchen
beschrieben
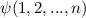 eines
Systems aus
eines
Systems aus 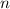 (wechselwirkenden) Teilchen (Elektronen) erfüllt die
Austauschsymmetrie, wenn beim beliebigen Tausch zweier Teilchen
(Elektronen) die Wahrscheinlichkeitsdichte
(wechselwirkenden) Teilchen (Elektronen) erfüllt die
Austauschsymmetrie, wenn beim beliebigen Tausch zweier Teilchen
(Elektronen) die Wahrscheinlichkeitsdichte 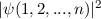 unverändert bleibt.
Diese Forderung der Austauschsymmetrie kann durch die Konstruktion von
symmetrischen (bleiben unverändert bei der Vertauschung zweier Teilchen) und
antisymmetrischen (ändern das Vorzeichen bei der Vertauschung zweier
Teilchen) Wellenfunktionen erfüllt werden.
unverändert bleibt.
Diese Forderung der Austauschsymmetrie kann durch die Konstruktion von
symmetrischen (bleiben unverändert bei der Vertauschung zweier Teilchen) und
antisymmetrischen (ändern das Vorzeichen bei der Vertauschung zweier
Teilchen) Wellenfunktionen erfüllt werden.
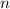 ,
, 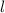 ,
, 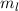 und
und 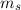 beschrieben. Alle Zustände, die zu einer
festen Hauptquantenzahl
beschrieben. Alle Zustände, die zu einer
festen Hauptquantenzahl 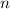 gehören, bilden dabei eine Schale, alle Zustände,
die zu einer festen Bahndrehimpulsquantenzahl
gehören, bilden dabei eine Schale, alle Zustände,
die zu einer festen Bahndrehimpulsquantenzahl 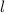 gehören, bilden eine
Unterschale und die Besetzung der Elektronenzustände und damit der Schalen
und Unterschalen von Atomen durch Elektronen erfolgt nach zwei
Prinzipien:
gehören, bilden eine
Unterschale und die Besetzung der Elektronenzustände und damit der Schalen
und Unterschalen von Atomen durch Elektronen erfolgt nach zwei
Prinzipien:
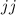 -Kopplung unterschieden.
-Kopplung unterschieden.
Bei der Russell-Saunders-Kopplung (leichte Atome) ist die Coulomb-Wechselwirkung
viel grösser als die Spin-Bahn-Kopplung und die Bahndrehimpulse 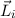 der
einzelnen Elektronen koppeln zu einem Gesamtbahndrehimpuls
der
einzelnen Elektronen koppeln zu einem Gesamtbahndrehimpuls 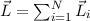 ,
wobei
,
wobei 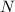 die Anzahl der Elektronen bezeichnet. Analog koppeln die Spins
die Anzahl der Elektronen bezeichnet. Analog koppeln die Spins 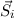 der einzelnen Elektronen zu einem Gesamtspin
der einzelnen Elektronen zu einem Gesamtspin 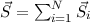 . Der resultierende
Gesamtbahndrehimpuls
. Der resultierende
Gesamtbahndrehimpuls 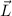 wechselwirkt dann mit dem Gesamtspin
wechselwirkt dann mit dem Gesamtspin 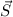 und bestimmt so den Gesamtdrehimpuls
und bestimmt so den Gesamtdrehimpuls 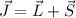 . Der Betrag der
Drehimpulse
. Der Betrag der
Drehimpulse 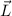 ,
, 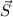 und
und 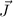 ist dabei auf die gleiche Art und Weise wie beim
Wasserstoffatom quantisiert. Sie sind bestimmt durch die Quantenzahlen
ist dabei auf die gleiche Art und Weise wie beim
Wasserstoffatom quantisiert. Sie sind bestimmt durch die Quantenzahlen
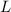 ,
,  und
und 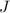 gemäss
gemäss 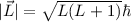 ,
,  und
und
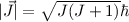 .
.
Bei der 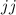 -Kopplung (schwere Atome) ist die Coulomb-Wechselwirkung viel
kleiner als die Spin-Bahn-Kopplung der einzelnen Elektronen. Es ist dann nicht
mehr möglich einen Gesamtbahndrehimpuls
-Kopplung (schwere Atome) ist die Coulomb-Wechselwirkung viel
kleiner als die Spin-Bahn-Kopplung der einzelnen Elektronen. Es ist dann nicht
mehr möglich einen Gesamtbahndrehimpuls 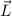 und einen Gesamtspin
und einen Gesamtspin 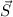 zu
definieren, sondern die Bahndrehimpulse
zu
definieren, sondern die Bahndrehimpulse 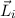 und Spins
und Spins 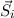 der einzelnen
Elektronen koppeln einzeln zu einem Gesamtdrehimpuls
der einzelnen
Elektronen koppeln einzeln zu einem Gesamtdrehimpuls 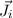 der einzelnen
Elektronen und diese wiederum zu einem Gesamtdrehimpuls
der einzelnen
Elektronen und diese wiederum zu einem Gesamtdrehimpuls 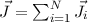 . In
der Realität liegt bei den meisten Atomen eine Mischform zwischen
Russell-Saunders- und
. In
der Realität liegt bei den meisten Atomen eine Mischform zwischen
Russell-Saunders- und 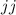 -Kopplung vor.
-Kopplung vor.
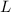 , Gesamtspinquantenzahl
, Gesamtspinquantenzahl
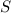 und Gesamtdrehimpulsquantenzahl
und Gesamtdrehimpulsquantenzahl 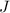 die Bezeichnung
die Bezeichnung 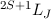 verwendet, wobei für
verwendet, wobei für 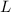 jeweils der entsprechende Grossbuchstabe
einzusetzen ist. Bei Atomen mit einem einzigen Elektron in der äussersten
Unterschale wird die Hauptquantenzahl
jeweils der entsprechende Grossbuchstabe
einzusetzen ist. Bei Atomen mit einem einzigen Elektron in der äussersten
Unterschale wird die Hauptquantenzahl 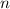 dieses Elektrons der Bezeichnung
vorangestellt.
dieses Elektrons der Bezeichnung
vorangestellt.
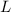 ,
, 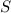 und
und  für ein Atom im
Grundzustand sind durch die nach Friedrich Hund benannten Hundschen
Regeln bestimmt:
für ein Atom im
Grundzustand sind durch die nach Friedrich Hund benannten Hundschen
Regeln bestimmt:
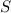 nimmt den maximal möglichen Wert
an.
nimmt den maximal möglichen Wert
an.
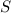 ,
liegt derjenige mit maximaler Gesamtbahndrehimpulsquantenzahl
,
liegt derjenige mit maximaler Gesamtbahndrehimpulsquantenzahl
 energetisch am tiefsten.
energetisch am tiefsten.
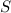 und
maximaler Gesamtbahndrehimpulsquantenzahl
und
maximaler Gesamtbahndrehimpulsquantenzahl 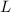 bildet bei weniger
als halbgefüllten Schalen der Zustand mit
bildet bei weniger
als halbgefüllten Schalen der Zustand mit  (minimales
(minimales
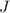 ) den Grundzustand, sonst der Zustand mit
) den Grundzustand, sonst der Zustand mit 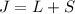 (maximales
(maximales 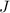 ).
).Zum Teil wird auch die Regel, dass für abgeschlossene Unterschalen
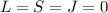 ist, als weitere Hundsche Regel aufgeführt.
ist, als weitere Hundsche Regel aufgeführt.